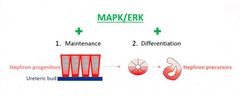
Syöpäsignaalit säätelevät munuaisen normaalia kehitystä
Munuaissairaudet yleistyvät länsimaissa muun muassa diabeteksen räjähdysmäisen kasvun myötä. Lisäksi munuaisten puute, virtsajohtimen häiriöt ja munuaissyöpä ovat tavallisimpia synnynnäisiä kehityshäiriöitä, ja niitä tavataan noin prosentilla vastasyntyneistä vauvoista.
Yleisestä esiintyvyydestä huolimatta munuaisen kehityshäiriöiden syntymekanismit tunnetaan huonosti ja munuaissairauksista kärsiviä potilaita hoidetaan dialyysin ja lopulta munuaissiirteen avulla. Molemmat hoitomenetelmät heikentävät potilaan elämänlaatua huomattavasti, eikä luovutettuja munuaisia löydy kaikille tarvitseville.
Munuaishäiriöiden diagnostiikan parantaminen sekä uusien hoitomenetelmien kehittäminen vaatii yksityiskohtaista tietoa munuaisen kehityksen säätelymekanismeista. Askeleen lähemmäksi tätä päästiin, kun Helsingin yliopiston tutkijat selvittivät, että syöpäsoluissa useasti muuntunut MAPK-signalointi osallistuu normaalin yksilönkehityksen aikana munaisen toiminnallisten yksiköiden, nefroneiden, lopullisen määrän kontrollointiin.
MAPK-signalointi välittää solun ulkopuolelta tulevien kasvutekijöiden vaikutuksen solun sisäisiin osiin. Sen tehtävät jakautuvat tumassa tapahtuvaan DNA:n aktivaation hallintaan ja solulimassa toteutuvaan proteiinien toiminnan säätelyyn.
Stem Cell Reports -lehdessä julkaistussa tutkimuksessa osoitettiin, että solujen jakautumisen säätelyyn usein liitetty MAPK-signalointi säätelee nefroneiden kantasolujen kommunikaatiota ympäristönsä kanssa. Sitä tarvitaan solujen normaaliin erilaistumiseen.
– Tulokset paljastavat, että MAPK-signalointi osallistuu solujen välisten sidosten jatkuvaan muokkaamiseen, mikä mahdollistaa niiden kasvun ja liikkumisen. Se liittyy munuaisen kehityksen aikaiseen muodonmuutokseen, sanoo tutkimusta johtanut Satu Kuure Helsingin yliopistosta.
MAPK-signalointiin vaikuttavia lääkkeitä on käytetty syöpähoidoissa jo pitkään. Nyt raportoitu tutkimus tuo toivoa myös kantasoluterapiaan perustuvien hoitomuotojen kehittämiseen.
– Lääkkeiden avulla voidaan kontrolloidusti käynnistää ja hiljentää MAPK-signalointi. Tätä oikea-aikaisesti hyödyntämällä on mahdollista, että elinten erilaistamista voidaan huomattavasti tehostaa, Kuure sanoo.
Alkuperäinen julkaisu:
Anneliis Ihermann-Hella et al. Dynamic MAPK/ERK activity sustains nephron progenitors through niche regulation and primes precursors for differentiation, Stem Cell Reports, DOI: 10.1016/j.stemcr.2018.08.012
Yhteystiedot:
Satu Kuure, lääketieteellinen tiedekunta & HiLIFE, Helsingin yliopisto, satu.kuure@helsinki.fi, puh. 02941 59395
Avainsanat
Yhteyshenkilöt
Elisa LautalaViestinnän asiantuntija
Puh:+358 50 318 5682elisa.lautala@helsinki.fiKuvat
Linkit
Tietoja julkaisijasta
 Helsingin yliopisto
Helsingin yliopistoPL 3
00014 Helsingin yliopisto
02941 22622 (mediapalvelu) 02941 911 (vaihde) (vaihde)https://www.helsinki.fi/fi/yliopisto
Helsingin yliopisto on yli 40 000 opiskelijan ja työntekijän kansainvälinen yhteisö, joka tuottaa tieteen voimalla kestävää tulevaisuutta koko maailman parhaaksi. Kansainvälisissä yliopistovertailuissa Helsingin yliopisto sijoittuu maailman parhaan yhden prosentin joukkoon. Monitieteinen yliopisto toimii neljällä kampuksella Helsingissä sekä Lahden, Mikkelin ja Seinäjoen yliopistokeskuksissa. Lisäksi sillä on kuusi tutkimusasemaa eri puolilla Suomea ja yksi Keniassa. Yliopisto on perustettu vuonna 1640.
Tilaa tiedotteet sähköpostiisi
Haluatko tietää asioista ensimmäisten joukossa? Kun tilaat tiedotteemme, saat ne sähköpostiisi välittömästi julkaisuhetkellä. Tilauksen voit halutessasi perua milloin tahansa.
Lue lisää julkaisijalta Helsingin yliopisto
Eduskuntavaalitutkimus 2023 julkistamistilaisuus 13.5. Helsingin yliopiston valtiotieteellisessä tiedekunnassa25.4.2024 11:02:23 EEST | Kutsu
Lämpimästi tervetuloa ”Pääministerivaalit polarisaation aikakaudella: Eduskuntavaalitutkimus 2023” julkistamistilaisuuteen 13.5. klo 10-12 . Nyt julkaistava eduskuntavaalitutkimuksen pääraportti on kattava teos suomalaisten äänestäjien käyttäytymisestä 2023 eduskuntavaaleissa.
Iäkkäiden lääkehoidon riskitekijöiden tunnistaminen on avainasemassa kotona asumisen tukemisessa23.4.2024 09:58:40 EEST | Tiedote
Tuoreessa väitöstutkimuksessa on kehitetty malli iäkkäiden lääkehoidon riskitekijöiden tunnistamiseksi osana laajempaa terveystarkastusta. Tutkimuksen tavoitteena oli tarjota konkreettisia keinoja iäkkäiden terveyden ja toimintakyvyn ylläpitämiseksi, jotta he voisivat asua kotona mahdollisimman pitkään.
Helsingin yliopiston operatiivinen tulos 2023 oli 16 miljoonaa euroa miinuksella17.4.2024 14:37:06 EEST | Tiedote
Varainhankinta sekä sijoitus- ja rahoitustuotot nostivat kokonaistuloksen plussalle. Yliopisto lisää sijoitustoiminnan tuotonjakoa perustehtävään seuraavien viiden vuoden ajan.
Pelastakaa tiede! -dokumenttielokuva kertoo tieteen evakuoinnin tarinan17.4.2024 10:28:01 EEST | Tiedote
Kirjailija, FT Anna Kortelainen, Kansalliskirjasto ja Kirjastokaista ovat tuottaneet yhteistyössä dokumentin, joka pureutuu Kansalliskirjaston aineistojen evakuointiin talvi- ja jatkosodan aikana. Elokuva julkaistaan 17.4.2024 Kirjastokaistan verkkosivuilla sekä Kansalliskirjaston Youtube-kanavalla.
Kutsu medialle: Tule seuraamaan Viikin tutkimustilan lehmien keväistä laitumellelaskua 4.5.!15.4.2024 14:44:21 EEST | Tiedote
Helsingin yliopisto, Valio ja maatalousylioppilaiden yhdistys Sampsa kutsuvat median edustajat osallistumaan Suomen urbaanimpien lehmien laitumellelaskuun Viikin tutkimustilalla lauantaina 4. toukokuuta.
Uutishuoneessa voit lukea tiedotteitamme ja muuta julkaisemaamme materiaalia. Löydät sieltä niin yhteyshenkilöidemme tiedot kuin vapaasti julkaistavissa olevia kuvia ja videoita. Uutishuoneessa voit nähdä myös sosiaalisen median sisältöjä. Kaikki tiedotepalvelussa julkaistu materiaali on vapaasti median käytettävissä.
Tutustu uutishuoneeseemme